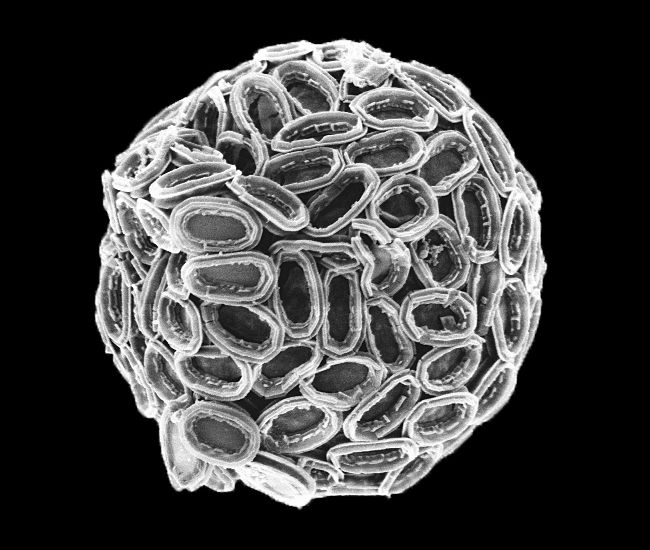
Nun haben Wissenschafter beobachtet, wie die Kalkalge Pleurochrysis carterae ihre winzigen Kalkschuppen aufbaut.
Potsdam – Muscheln, Kalkalgen, aber auch Seeigel und Seesterne gelten als hervorragende Nano-Baumeister: Allein mit Kalk, Proteinen und Zuckern erschaffen sie winzige, präzise geformte Strukturen. Wie sie das zuwege bringen, ist noch immer nicht vollständig geklärt. Nun haben deutsche Wissenschafter einen entscheidenden Mechanismus entdeckt, wie eine Kalkalge die filigranen Konstruktionen erzeugt. Die neuen Erkenntnisse könnten sich sogar technisch nutzen lassen.
Obwohl selbst die schwersten Exemplare der Kalkalgen weniger als ein Milliardstel Gramm wiegen, produzieren diese Einzeller allein weltweit Calciumcarbonat mit einer Masse von bis zu 500 Millionen Tonnen. Das entspricht etwa einem Drittel der globalen Stahlproduktion pro Jahr. Mit dem Kalk in Form von einigen Nanometer großen Calcitkristallen errichten sie wahre architektonische Meisterwerke. "Wir haben nun einen biochemischen Mechanismus entdeckt, der bewirkt, dass sich die Kristalle dort bilden, wo sie gebraucht werden", sagt André Scheffel, Forscher am Max-Planck-Institut für molekulare Pflanzenphysiologie und Hauptautor der aktuellen Studie.
Untersucht hat das Forscherteam die Kalkalge Pleurochrysis carterae. Sie gehört zu den Coccolithophoriden, einer Gruppe von einzelligen Meeresalgen, die ihren Namen den Kalkschuppen – Coccolithen genannt – auf ihrer Oberfläche verdanken. Diese winzigen Kalkschuppen besitzen eine Bodenplatte, die aus organischem Material, vor allem Cellulosefasern, besteht und wie ein Tortenboden von einem Rand eingefasst wird. An diesem Rand, und nur dort, sind abwechselnd Calcit-Kristalle mit zwei unterschiedlichen Formen angeordnet. Die Coccolithen werden im Inneren der Zelle in einem speziellen Vesikel, einem von einer Membran umschlossenen Raum, gebildet. Die fertigen Coccolithen werden dann aus der Zelle ausgeschleust und im Coccolithenpanzer integriert, der jede Algenzelle umgibt.
Zucker übernimmt den Calciumtransport
"Wie sich die regelmäßige Struktur in dem speziellen Membranraum bildet, war bislang unklar", sagt Scheffel. "Bislang hielt man die chemische Struktur der Bodenplatte für ausschlaggebend, damit sich die Kalk-Kristalle nur am Rand der Coccolithen bilden." Ein Irrtum wie Versuchen im Reagenzglas zeigten. "Damit die Kalk-Kristalle an der richtigen Stelle entstehen, kommt es interessanter Weise auf die löslichen negativ geladenen Vielfachzucker an", so Scheffel. Diese transportieren aber nur das positiv geladene Calcium und kein Calciumcarbonat zum Rand der Bodenplatte und lagern sich mit ihm dort in Form kleiner Klümpchen ab. Die Proteine sind an der Navigation demnach unbeteiligt. Frühere Untersuchungen hatten zwar ergeben, dass die löslichen Bestandteile bei der Kristallisation von Calciumcarbonat mitmischen. Welche Rolle Vielfachzucker und Proteine dabei genau spielen, war bislang aber nicht bekannt.
Wie die Forscher außerdem festgestellt haben, funktioniert die zielsichere Zustellung nur mit Calcium, andere Metallionen wie Magnesium oder Natrium verteilen die Polysaccharide wahllos auf der Bodenplatte oder liefern sie dort gar nicht ab. Diese Erkenntnisse sind wahrscheinlich nicht nur für P. carterae relevant, sondern für alle Organismen, die Kalk verarbeiten: andere Kalkalgen, Muscheln und Seeigel, glauben die Forscher. Dahinter zu kommen, wie Meerestiere Kalk-Konstruktionen bauen, könnte auch für technische Anwendungen nützlich sein. Die Kniffe der Natur können nämlich auch Materialwissenschaftern Anregungen geben, wie sich auf präzise Weise winzige Strukturen für die Nanotechnologie erzeugen lassen. (red, 14.8.2016)